Utveckling och framtid inom muskuloskeletal MR-diagnostik
Dagens magnetresonanstomografi (MR) inom det muskuloskeletala systemet domineras av morfologisk bildgivning utan närmare information om fysiologiska vävnadsegenskaper (ref 1). Under de senaste decennierna har nya MR-metoder utvecklats som erbjuder möjligheten att visualisera och kvantifiera funktion. Vissa används redan till exempel i MR-diagnostik av hjärnan, hjärtat eller levern, men inte inom det muskuloskeletala systemet trots att tekniska valideringsstudier har publicerats (ref 2).
MR utvecklas mot snabbare och mer specifika sekvenser, korta protokoll och mer kvantitativa metoder (ref 3). Nya snabba MR-sekvenser och nya rekonstruktionsalgoritmer kan minska undersökningstiden samtidigt som hög bildkvalitet bibehålls. Moderna 3- eller 7-Tesla MR-kameror har potentialen att maximera bildkvaliteten som är viktigt för att kunna visualisera små strukturer som handledens ligament och dess skador (ref 4, 5) jämfört med 1,5 T. Tredimensionell MR med planar reformation kan erbjuda möjligheten till rekonstruktion i alla plan som kan vara viktig för mer komplicerade leder som handled (ref 5) eller fotled (ref 6).
Den nuvarande förståelsen av det muskuloskeletala systemet begränsas av en kunskapslucka avseende det kliniska värdet av nya och avancerade MR metoder vid bedömning av tillstånd såsom tumörsjukdom, senpatologi, broskskador, eller skador på strukturer som utför ledstabilitet, som ligament eller menisk.
DIFFUSIONSVIKTAD MAGNETRESONANSAVBILDNING
Diffusionsviktad avbildning (DWI) gör det möjligt att bedöma diffusionen av vattenmolekyler i vävnader, vilket relaterar till bland annat celltätheten i den undersökta vävnaden. Den morfologiska grunden är det faktum att vattenmolekylernas diffusionsrörelse hindras av membran och makromolekyler i vävnad, vilket kan förväntas ske till högre grad i maligna förändringar som i sarkom som vanligtvis har en ökad celltäthet, jämfört med oförändrade vävnader och godartade förändringar (ref 2). Nyligen publicerade studier har, i linje med detta, visat att DWI har potential att göra det lättare att skilja mellan godartade och maligna förändringar i det muskuloskeletala systemet jämfört med konventionella MR-sekvenser (ref 7, 8).
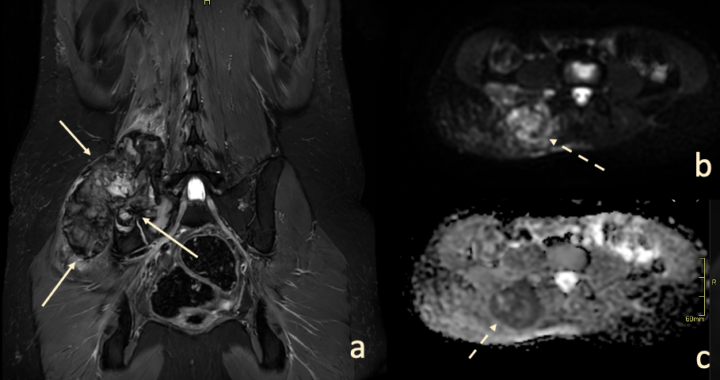
Användningen av DWI (Bild 1) skulle kunna minska behovet av kontrastmedel vid kontrollundersökningar efter tumöroperationer eftersom dagens diagnostik med konventionella MR-sekvenser till stor del bygger på bedömning av kontrastmedelsuppladdning i suspekta vävnader. DWI har dock sina begränsningar, bland annat på grund av magnetfältets inhomogenitet i ojämna områden av vår kropp (till exempel området kring axelleden där det finns en disproportion mellan dimensionerna av nacken och axlarna samt närvaron av rörliga lungor, stora kärl etc.) vilket leder till till exempel bildförvrängningar och artefakter. Diffusion är en känslig metod, men dess användning inom rörelseapparatens system är för närvarande inte stor, eftersom det saknas studier på större material.
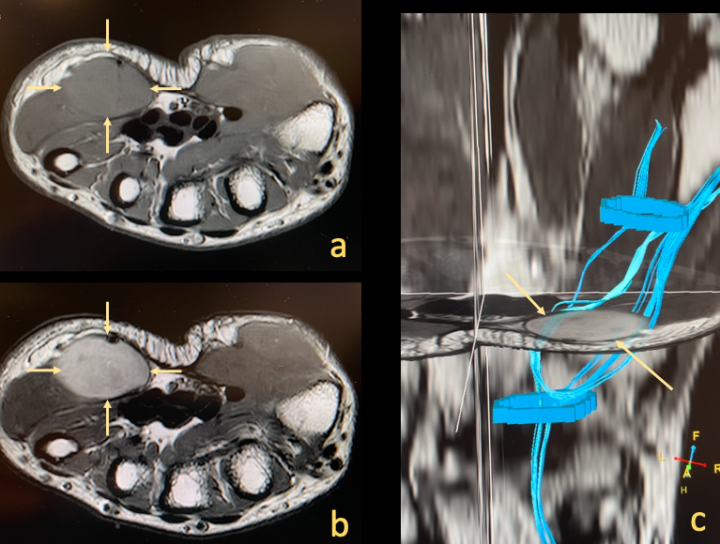
Diffusion tensor imaging (DTI; Bild 2) är en variant av DWI som syftar till att avbilda den riktningsberoende signalen hos vattenmolekylernas diffusion i vävnaden. Inom rörelseapparaten kan DTI används för att avbilda diffusionen längs muskelfibrer (ref 9) för att bedöma skador på muskler som inte är synliga i konventionella sekvenser, vilket kan vara av betydelse för att upptäcka mindre, interna muskelskador hos idrottare (ref 10, 11). I utredningen av tumörer i, eller i anslutning till, nerver kan DTI används för att bedöma huruvida diffusionen längs med nerven är påverkad och därmed ge information om nervens integritet (Bild 2). Detta är relevant i differential-diagnosen tex mellan nervtumörer och nervskidetumörer (ref 12) eller mellan lokalt växande och infiltrativa tumörer (ref 13, 14)
T2-VIKTADE SEKVENSER MED ULTRAKORT EKOTID (UTE)
Diagnostik av senor i konventionella MR-sekvenser som T2-viktade eller protondensitetsviktade (PD) sekvenser tillåter upptäckt av avancerade förändringar av senor på mikroskop är relaxationstiderna för senor och ligament betydligt kortare jämfört med muskler. Med UTE-sekvenser kan man på ett effektivt sätt upptäcka förändringar i senor och stora ligament, vilket används för diagnostiken i t.ex. hälsenan (ref 15, 16).
MR AV BROSK
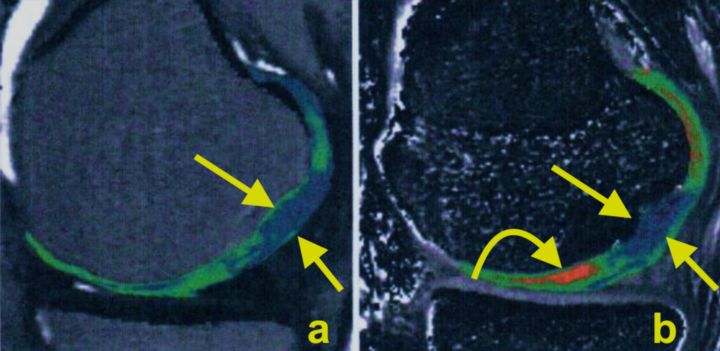
Bilddiagnostik av brosk med MR har genomgått en betydande teknisk utveckling. Rutinmässigt använda sekvenser, såsom PD-viktad avbildning med fettundertryckning och har kompletterats med nya sekvenser för en mer biokemisk broskbedömning. Anledningen till detta är att de tidigare använda sekvenserna endast kunde visualisera anatomiska defekter i broskets tjocklek och inte gav någon information om broskets biokemiska sammansättning. De nya avbildningsmetoderna kan i framtiden komma att användas som biomarkörer för sammansättningen av extracellulär broskmatrix. För att visualisera kollageninnehåll i brosk används T2-mapping och diffusion (ref 17; Bild 3). Proteoglykaner i brosk kan bedömas med T1 rho och delayed gadolinium-enhanced MRI of cartilage (dGEMRIC). Glykosaminoglykaner i brosk kan visualiseras genom användning av natrium-MR, glycosaminoglycan chemical exchange saturation transfer (gagCEST) och dGEMRIC. Genom att avbilda komponenter i extracellulär broskmatrix kan områden med patologiska förändringar i brosk identifieras tidigt, vilket inte är möjligt med konventionella sekvenser. De nya sekvenserna, särskilt T2-mapping, används för att utvärdera brosk som har genomgått kirurgiska ingrepp för att upptäcka potentiella komplikationer efter broskreparation (ref 18). T2-mapping och dGEMRIC används idag i klinisk rutin på många sjukhus, medan övriga tekniker i huvudsak är i forsknings-stadiet.
DYNAMISK MR
Dynamisk MR möjliggör bedömning av ledens funktion in vivo under rörelse. Genom denna avbildning kan stabiliteten hos strukturer såsom menisker, brosk, senor och ligament bedömas (ref 19). Dessa sekvenser, som visas som filmer, ger en värdefull insikt i ledens dynamiska aspekter, vilket inte är möjligt med rutinmässigt använda sekvenser. Med denna metod kan man bedöma hur fettvävnaden i knäet påverkas, hur korsbandsgraft fungerar efter operation och även noggrant bedöma meniskerna och meniskstabilitet. Genom denna metod kan skador på meniskers bakre rötter, som är mycket svåra att identifiera med konventionella sekvenser, upptäckas. På så sätt kan antalet förbisedda skador på rötterna minskas (ref 20). Att upptäcka sådana skador är avgörande för att förhindra utvecklingen av degenerativa förändringar.
MR-SPEKTROSKOPI (MRS)
MRS är en teknik som ger oss insikt i den biokemiska sammansättningen av den undersökta vävnaden och kan indikera patologiska processer innan dessa kan visualiseras med konventionella MR-metoder. En ökning av kolin, som är en cellmembransmarkör, kan till exempel indikera maligna processer med hög cellomsättning både i utrednings- och uppföljningsfasen av tumörpatienter (ref 21, 22). En annan tillämpning av MRS är att kvantifiera inlagringen av fett i skelettmuskulaturens intra- och extramyocellulära fettfack, vilket ger bättre kvantifiering av fettatrofi än konventionella sekvenser (ref 10).
SAMMANFATTNING
Den tekniska utvecklingen av MR har gjort många framsteg de senaste decennierna vilket har skapat möjligheter att tillämpa nya MR-sekvenser som kan främja diagnostiken inom tidigare svårbedömda områden i det muskuloskeletala systemet. De nya teknikerna har dessutom förändrat vår syn på diagnostik med hög precision då vi tidigare främst fokuserade på högkvalitativ morfologisk bildgivning medan funktionella aspekter i framtiden potentiellt kan synliggöra patologi, korta ner undersökningstider och reducera behovet av kontrastmedel. Emellertid finns det en brist på standardisering och klinisk validering av de nya undersökningarna vilket innebär att ytterligare studier behövs för att tillämpa de nya MR-sekvenserna i en klinisk vardag. Det är därför hög tid att en del av radiologisk diagnostik inom det muskuloskeletala systemet centraliseras och bedrivs med specialistkompetens för att kunna utnyttja den potential som den nya tekniken ger möjlighet till.
Pawel Szaro
Överläkare, Docent
Gustav Lodeiro
Läkarstudent
Katarzyna Bokwa-Dabrowska
Överläkare, PhD
Oscar Jalnefjord
Sjukhusfysiker, PhD
Isabella Björkman-Burtscher
Professor, Överläkare
Samtliga på avdelningen för radiologi
Sahlgrenska akademin, Göteborgs universitet och Sahlgrenska universitetssjukhuset Göteborg
Referenser
[1] P.J. Basser, C. Pierpaoli, Microstructural and physiological features of tissues elucidated by quantitative-diffusion-tensor MRI, J Magn Reson B 111(3) (1996) 209-19.
[2] H. Joint, M.R.I.D.C. Neck Radiotherapy, A.S.R. Mohamed, A. Abusaif, R. He, K.A. Wahid, V. Salama, S. Youssef, B.A. McDonald, M. Naser, Y. Ding, T.C. Salzillo, M.A. AboBakr, J. Wang, S.Y. Lai, C.D. Fuller, Prospective validation of diffusion-weighted MRI as a biomarker of tumor response and oncologic outcomes in head and neck cancer: Results from an observational biomarker pre-qualification study, Radiother Oncol 183 (2023) 109641.
[3] F. Del Grande, R. Guggenberger, J. Fritz, Rapid Musculoskeletal MRI in 2021: Value and Optimized Use of Widely Accessible Techniques, AJR Am J Roentgenol 216(3) (2021) 704-717.
[4] S. Gotestrand, A. Bjorkman, I.M. Bjorkman-Burtscher, I. Kristiansson, E. Aksyuk, P. Szaro, K. Markenroth Bloch, M. Geijer, Visualization of wrist anatomy-a comparison between 7T and 3T MRI, Eur Radiol 32(2) (2022) 1362-1370.
[5] S. Gotestrand, A. Bjorkman, I.M. Bjorkman-Burtscher, R. Ab-Fawaz, I. Kristiansson, B. Lundin, M. Geijer, Visualization of wrist ligaments with 3D and 2D magnetic resonance imaging at 3 Tesla, Acta Radiol 63(3) (2022) 368-375.
[6] R. Kijowski, J. Fritz, Emerging Technology in Musculoskeletal MRI and CT, Radiology 306(1) (2023) 6-19.
[7] S. Arslan, F.B. Ergen, G.B. Aydin, M. Ayvaz, J. Karakaya, K. Kosemehmetoglu, A.E. Yildiz, U. Aydingoz, Different Attenuation Models of Diffusion-Weighted MR Imaging for the Differentiation of Benign and Malignant Musculoskeletal Tumors, J Magn Reson Imaging 55(2) (2022) 594-607.
[8] Q. Wang, X. Xiao, Y. Liang, H. Wen, X. Wen, M. Gu, C. Ren, K. Li, L. Yu, L. Lu, Diagnostic Performance of Diffusion MRI for differentiating Benign and Malignant Nonfatty Musculoskeletal Soft Tissue Tumors: A Systematic Review and Meta-analysis, J Cancer 12(24) (2021) 7399-7412.
[9] C.C. Van Donkelaar, L.J. Kretzers, P.H. Bovendeerd, L.M. Lataster, K. Nicolay, J.D. Janssen, M.R. Drost, Diffusion tensor imaging in biomechanical studies of skeletal muscle function, J Anat 194 ( Pt 1)(Pt 1) (1999) 79-88.
[10] T. Nozaki, A. Tasaki, S. Horiuchi, C. Osakabe, S. Ohde, Y. Saida, H. Yoshioka, Quantification of Fatty Degeneration Within the Supraspinatus Muscle by Using a 2-Point Dixon Method on 3-T MRI, AJR Am J Roentgenol 205(1) (2015) 116-22.
[11] M. Froeling, J. Oudeman, G.J. Strijkers, M. Maas, M.R. Drost, K. Nicolay, A.J. Nederveen, Muscle changes detected with diffusion-tensor imaging after long-distance running, Radiology 274(2) (2015) 548-62.
[12] M. Kronlage, V. Schwehr, D. Schwarz, T. Godel, L. Uhlmann, S. Heiland, M. Bendszus, P. Baumer, Peripheral nerve diffusion tensor imaging (DTI): normal values and demographic determinants in a cohort of 60 healthy individuals, Eur Radiol 28(5) (2018) 1801-1808.
[13] K.I. Desai, The Surgical Management of Symptomatic Benign Peripheral Nerve Sheath Tumors of the Neck and Extremities: An Experience of 442 Cases, Neurosurgery 81(4) (2017) 568-580.
[14] E. Istefan, J. Belstock, L.B. Dahlin, E. Nyman, Surgery of Schwannoma in the upper limb - sensitivity and specificity of preoperative magnetic resonance imaging and relation between tumour size and symptoms, BMC Musculoskelet Disord 24(1) (2023) 713.
[15] A. Foure, New Imaging Methods for Non-invasive Assessment of Mechanical, Structural, and Biochemical Properties of Human Achilles Tendon: A Mini Review, Front Physiol 7 (2016) 324.
[16] M.D. Robson, M. Benjamin, P. Gishen, G.M. Bydder, Magnetic resonance imaging of the Achilles tendon using ultrashort TE (UTE) pulse sequences, Clin Radiol 59(8) (2004) 727-35.
[17] M.E. Buchanan, B.K. Markhardt, Systematic review of techniques in cartilage imaging, Journal of Cartilage & Joint Preservation (2023).
[18] M.A.I. Alsayyad, K.A. Ali Shehata, R.T. Khattab, Role of adding T2 mapping sequence to the routine MR imaging protocol in the assessment of articular knee cartilage in osteoarthritis, Egyptian Journal of Radiology and Nuclear Medicine 52(1) (2021).
[19] A.A.A. Qardash, A.A. Hassan, H.A. El kady, H.E.-D.G. Mohammed, M. Abdel-Tawab, N.A.A. Mohammed, Varus stress MRI in diagnosis of medial meniscal posterior root tear, Egyptian Journal of Radiology and Nuclear Medicine 53(1) (2022).
[20] X. Li, Q. Hou, X. Zhan, L. Chang, X. Ma, H. Yuan, The accuracy of MRI in diagnosing and classifying acute traumatic multiple ligament knee injuries, BMC Musculoskelet Disord 23(1) (2022) 43.
[21] P.A. Gondim Teixeira, M. Ledrich, F. Kauffmann, J.M. Wamba, J. Felblinger, A. Blum, G. Hossu, Qualitative 3-T Proton MR Spectroscopy for the Characterization of Musculoskeletal Neoplasms: Update on Diagnostic Performance and Indications, AJR Am J Roentgenol 208(6) (2017) 1312-1319.
[22] F.M. Costa, P.H. Martins, C. Canella, F. Lopes, Multiparametric MR Imaging of Soft Tissue Tumors and Pseudotumors, Magn Reson Imaging Clin N Am 26(4) (2018) 543-558.